2026年4月28日3Shape宣布,美国食品药品监督管理局(FDA)已批准其Dx软件上市,审查于2026年4月10日完成。
该510(k)上市前通知允许Dx(R1)软件在美国商业化,供合格牙科专业人员在牙科诊所使用,以辅助诊断关键口腔健康状况并评估成年患者牙齿和牙龈的变化。
3Shape首席执行官Jacob Paulsen表示:"我很高兴我们现在可以将这一变革性的牙科解决方案带给全美医生和患者。获得FDA 510(k)批准彰显了我们对负责任创新的承诺,以及提供满足最高临床和监管标准的数字解决方案的决心。借助Dx软件,牙科专业人员获得了一种强大的新方式,可以更清晰地向患者传达其口腔健康状况和治疗需求。"
FDA批准适用于3Shape Dx软件的两个版本:Dx Plus和Dx Standard。Dx Plus专为3Shape TRIOS 6扫描仪设计,是一款AI辅助软件,可辅助检测关键口腔健康状况,包括牙面和邻面龋、牙菌斑、牙齿磨损和牙龈退缩。Dx Standard软件可帮助牙医通过手动追踪和量化患者牙列的变化来吸引患者参与。该版本兼容除TRIOS Core外的所有3Shape TRIOS型号。
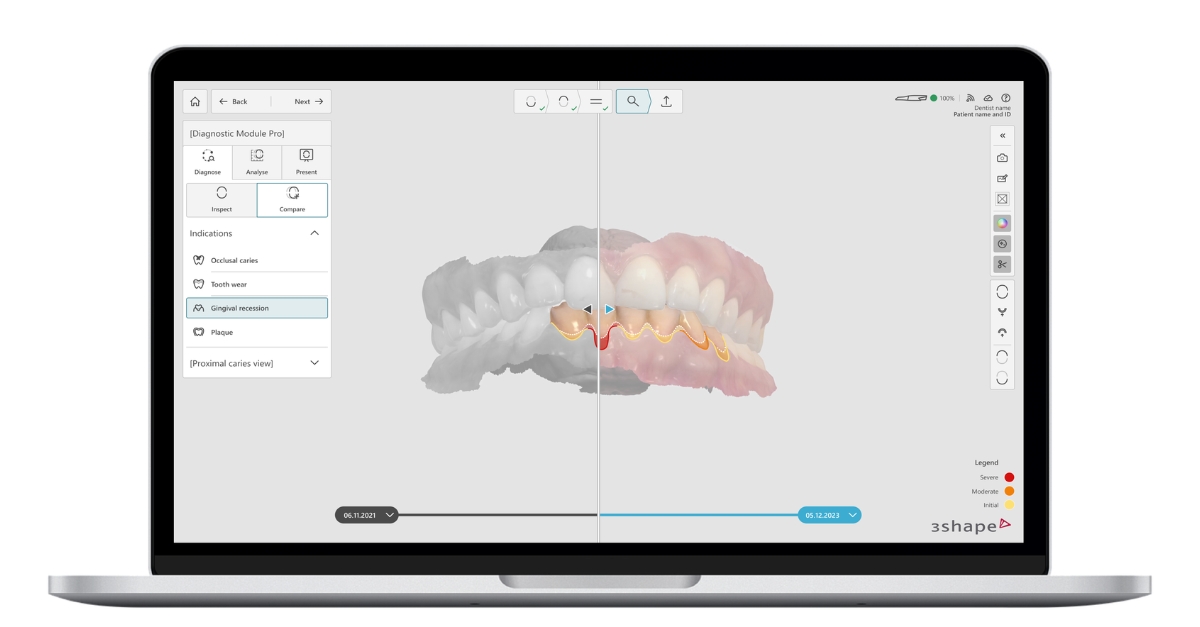
Dx支持常规检查,并可在为患者就诊做准备时节省时间。使用Dx,牙医可以在屏幕上与患者一起可视化关键口腔健康状况,并长期监测这些状况。Dx Plus可视化功能将临床发现转化为清晰、直观的视觉图像,帮助患者更好地理解诊断,建立对临床医生的信任,并对推荐的治疗方案更有信心。
FDA批准意味着Dx软件现在可以在美国向牙科专业人员推广和销售。自2025年以来,Dx软件已在包括欧洲、中东、非洲、南美洲和加拿大在内的多个国际市场销售和使用。
3Shape的Dx软件即日起在美国上市。请联系您的经销商或3Shape代表以获取购买信息。符合条件的客户可访问webshop.3shape.com开始试用。